Thérapies innovantes dans les leucémies myéloïdes et les cellules souches hématopoïétiques
151, Route de Saint-Antoine de Ginestière, BP2 3194 - NiceSite web - auberger@unice.fr -
Responsable d'équipe
Dr. Patrick Auberger

Thématiques de recherche
Notre équipe de recherche est rattachée au sein du Centre Méditerranéen de Médecine Moléculaire à Nice (INSERM-U1065). Nos thématiques de recherche concernent la genèse, la différenciation et la transformation des cellules myéloïdes. Nos projets de recherche s’articulent autour de 3 axes principaux : Le premier concerne le rôle du stress oxydatif dans la maintenance, la prolifération et la prise de greffe des cellules souches hématopoïétiques. Notre deuxième axe de recherche étudie le rôle des caspases et de l’autophagie dans les mécanismes de différenciation des monocytes en macrophages et dans les processus de polarisation de ces macrophages. Finalement, notre dernier axe de recherche analyse l’implication des lysosomes et des différentes formes d’autophagie dans les leucémies myéloïdes et le développement des SMD en LAM.
Figure descriptive
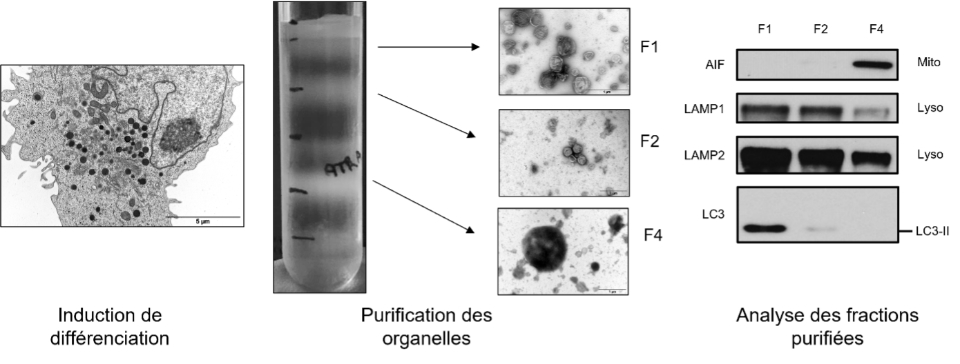
Publications
1. Zerhouni, M.; Martin, A.R.; Furstoss, N.; Gutierrez, V.S.; Jaune, E.; Tekaya, N.; Beranger, G.E.; Abbe, P.; Regazzetti, C.; Amdouni, H.; et al. Dual Covalent Inhibition of PKM and IMPDH Targets Metabolism in Cutaneous Metastatic Melanoma. Cancer Res 2021, 81, 3806–3821, doi:10.1158/0008-5472.CAN-20-2114.
2. Klionsky, D.J.; Abdel-Aziz, A.K.; Abdelfatah, S.; Abdellatif, M.; Abdoli, A.; Abel, S.; Abeliovich, H.; Abildgaard, M.H.; Abudu, Y.P.; Acevedo-Arozena, A.; et al. Guidelines for the Use and Interpretation of Assays for Monitoring Autophagy (4th Edition)1. Autophagy 2021, 17, 1–382, doi:10.1080/15548627.2020.1797280.
3. Robert, G.; Jacquel, A.; Auberger, P. Chaperone-Mediated Autophagy and Its Emerging Role in Hematological Malignancies. Cells 2019, 8, E1260, doi:10.3390/cells8101260.
4. Auberger P, Puissant A. Autophagy, a key mechanism of oncogenesis and resistance in leukemia. Blood. 2017 Feb. 2;129(5):547-552. PMID: 27956388.
5. Hamouda, M. A.; Jacquel, A.; Robert, G.; Puissant, A.; Richez, V.; Cassel, R.; Fenouille, N.; Roulland, S.; Gilleron, J.; Griessinger, E.; et al. BCL-B (BCL2L10) Is Overexpressed in Patients Suffering from Multiple Myeloma (MM) and Drives an MM-like Disease in Transgenic Mice. J Exp Med 2016, 213, 1705–1722, doi:10.1084/jem.20150983.
6. Obba, S.; Hizir, Z.; Boyer, L.; Selimoglu-Buet, D.; Pfeifer, A.; Michel, G.; Hamouda, M.-A.; Gonçalvès, D.; Cerezo, M.; Marchetti, S.; et al. The PRKAA1/AMPKα1 Pathway Triggers Autophagy during CSF1-Induced Human Monocyte Differentiation and Is a Potential Target in CMML. Autophagy 2015, 11, 1114–1129, doi:10.1080/15548627.2015.1034406.
Composition de l'équipe
Dr. Patrick Auberger, DRCE INSERM, auberger@unice.frDr. Guillaume Robert, CRCN INSERM
Dr. Arnaud Jacquel, CRCN INSERM
Dr. Marie-Laure Arcangeli, CRCN INSERM
Pr. Thomas Cluzeau, PU-PH (Hospitalier)
Pr. Nicolas Mounier, PU-PH (Hospitalier)
Dr. Michael Loschi, Chef de clinique (Hospitalier)
Coline Savy, IE CDD INSERM
Maxence Bourgoin, IE CDD INSERM
Cécile Favreau, IE CDD INSERM
Julie Bianco, IE CDD CHU
Paul Chaintreuil, Doctorant
Emeline Kerreneur, Doctorante